查看更多

 明星当前產品
明星当前產品
 幹貨推薦
幹貨推薦
 關注我們
關注我們

掃碼關注我們
了解更多信息
肝缺血再灌注損傷(Hepatic Ischemia/Reperfusion Injury, HIRI)是指在肝髒經曆一段時間的缺血後,恢複血液供應時導致的肝髒損傷。這一過程在肝髒移植、部分肝切除術以及出血性休克等臨床場景中不可避免,是導致早期移植物失敗的主要原因之一。既往研究表明HIRI的嚴重程度呈現時間依賴性:不同時間點進行缺血再灌注手術,肝髒損傷的嚴重程度會有所不同。這種時間依賴性提示了生物節律(晝夜節律)在HIRI中的潛在調控作用。基于這一背景,本研究聚焦于HIRI的晝夜節律調控,首次揭示了生物鍾-代謝-自噬這一分子軸在其中的關鍵作用,爲臨床防治HIRI提供了新策略。

2025年3月,大連醫科大學陳麗紅教授、管又飛教授和上海健康醫學院楊光銳教授團隊合作,在國際肝髒病學期刊Journal of Hepatology發表了題爲“Circadian Control of Hepatic Ischemia/Reperfusion Injury via HSD17B13-Mediated Autophagy in Hepatocytes”的研究論文,揭示了HIRI的晝夜節律調控機制。研究發現,夜間手術比早晨導致更嚴重的肝損傷,核心生物鍾轉錄因子BMAL1被鑒定爲這一節律性損傷的關鍵調控者。BMAL1通過直接調控肝細胞中17β-羟基類固醇脫氫酶13(HSD17B13)表達來影響HIRI。機制上,BMAL1-HSD17B13軸通過促進肝細胞自噬和減少脂質積累發揮保護作用,且該調控具有顯著的時間依賴性。本研究闡明了BMAL1/HSD17B13信號通路在肝細胞自噬和脂質代謝中的關鍵作用,是調控HIRI晝夜節律的核心通路。這些研究結果不僅加深了對HIRI發病機制的理解,更爲開發基于時間療法的新策略(如優化手術時機或靶向HSD17B13的治療幹預)提供了重要的理論基礎。
在本研究中,漢恒生物有幸爲作者提供了AAV2/9-TBG-shBmal1和AAV2/9-TBG-shHSD17B13,成功實現了小鼠肝細胞中Bmal1和HSD17B13的特異性敲低。
下面,我們一起來了解具體的研究內容:
研究成果
1.小鼠的HIRI呈現晝夜節律變化
Bmal1作爲核心生物鍾基因,在肝髒中表現出強烈的晝夜節律:其表達峰值出現在黎明(ZT0,光照開始),表達低谷出現在黃昏(ZT12,光照結束),分別標志着小鼠靜息期和活動期的起始。爲探究BMAL1在HIRI中的作用,作者分別在ZT0和ZT12時間點對野生型小鼠實施缺血/再灌注(I/R)手術。結果顯示ZT12-IRI組小鼠血清ALT/AST水平、肝組織壞死面積、凋亡相關蛋白表達及凋亡細胞數量等肝損傷指標均顯著高于ZT0-IRI組,提示BMAL1低表達可能促進凋亡。除此之外,炎症反應與氧化應激也存在晝夜差異:ZT12-IRI組肝髒中CD68⁺巨噬細胞和LY6G⁺中性粒細胞浸潤更顯著、促炎因子(Ccl2、Il1β等)及血清MPO水平更高,表明炎症反應更強;ROS生成增加,抗氧化酶(GSH、SOD)活性降低,表明氧化應激加劇。上述結果表明,HIRI的嚴重程度具有晝夜差異性,提示生物鍾基因可能通過調控凋亡和炎症通路影響HIRI進展。

圖1. HIRI在小鼠中呈現晝夜節律變化
2. 肝細胞中Bmal1敲除可消除HIRI晝夜差異並加劇肝損傷
隨後,作者通過兩種模型(肝細胞特異性敲低和敲除Bmal1)驗證肝細胞BMAL1是否介導HIRI的晝夜節律。結果顯示在肝細胞特異性Bmal1敲低/敲除模型中,ZT0-IRI組的損傷指標、炎症以及氧化應激水平與ZT12-IRI組相當,完全消除了晝夜差異。在敲除模型中,作者發現BMAL1通過調控三重通路發揮保護作用:①抑制氧化應激(降低ROS,維持GSH/SOD活性);②減輕炎症反應(減少中性粒細胞浸潤和促炎因子釋放);③調控細胞凋亡(維持BAX/BCL2平衡)。綜上結果表明肝細胞的BMAL1是HIRI晝夜節律的核心調控因子,其缺失通過加劇氧化應激、炎症和凋亡水平,消除了ZT0時段的損傷保護作用。
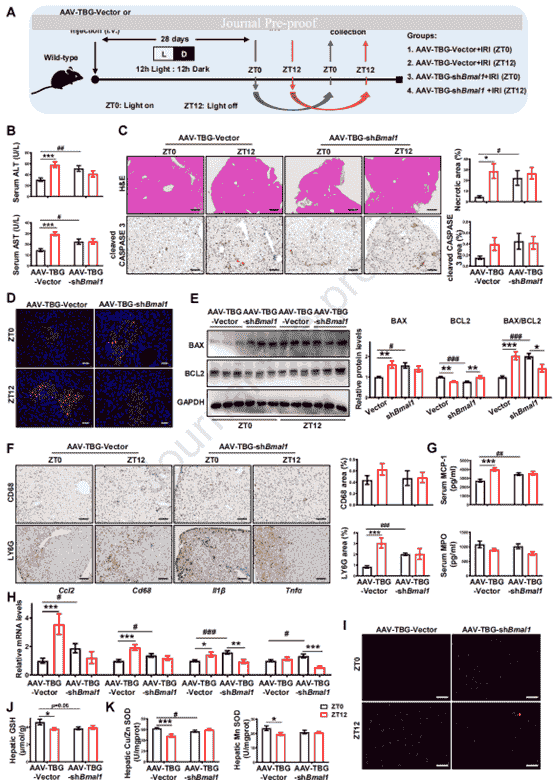
圖2. 肝細胞中BMAL1的敲低消除了HIRI的晝夜變化並加劇了肝損傷

圖3. 肝細胞中BMAL1的敲除加劇了肝損傷
3. HIRI小鼠肝組織的轉錄組學分析及核心分子機制驗證
爲了探索BMAL1介導HIRI晝夜節律變化及其保護肝髒的潛在機制,作者對HIRI模型小鼠的肝組織進行了轉錄組學分析。結果顯示,ZT12-IRI與ZT0-IRI組間共鑒定出1396個差異表達基因。功能富集分析顯示,上調基因主要涉及細胞損傷修複通路,與觀察到的肝損傷嚴重程度一致。而下調基因則富集于脂質代謝關鍵通路,表明ZT12-IRI小鼠存在肝髒代謝功能嚴重紊亂。進一步聚焦脂代謝相關DEG,發現 Hsd17b家族基因在ZT12組顯著下調,而其中HSD17B13作爲脂滴關聯蛋白,在既往研究中已被證實在脂肪性肝病中發揮關鍵作用。基于此,作者提出了核心假設:在肝細胞Bmal1敲低/敲除小鼠中觀察到的晝夜變化減弱和肝損傷加重由Hsd17b13表達節律失調介導。
爲了證實這一假設,作者分析了小鼠肝髒中HSD17B13的晝夜表達模式。結果顯示,在健康小鼠中HSD17B13呈現顯著的晝夜節律表達(ZT0達峰值,ZT12爲低谷,與Bmal1表達模式一致),且這一節律在Bmal1敲除小鼠中完全消失,表明Bmal1可能調節HSD17B13的晝夜表達。而HIRI組不僅顯著降低HSD17B13蛋白水平,還破壞了其晝夜節律性調控。隨後,作者通過荧光素酶報告實驗和染色質免疫沉澱(ChIP)進一步證明,BMAL1通過直接結合Hsd17b13啓動子區的E-box樣元件激活其轉錄,維持HSD17B13的晝夜節律性表達。以上結果共同表明BMAL1通過直接結合Hsd17b13啓動子調控其晝夜節律表達,該調控軸的破壞可能是HIRI晝夜差異的核心分子機制。
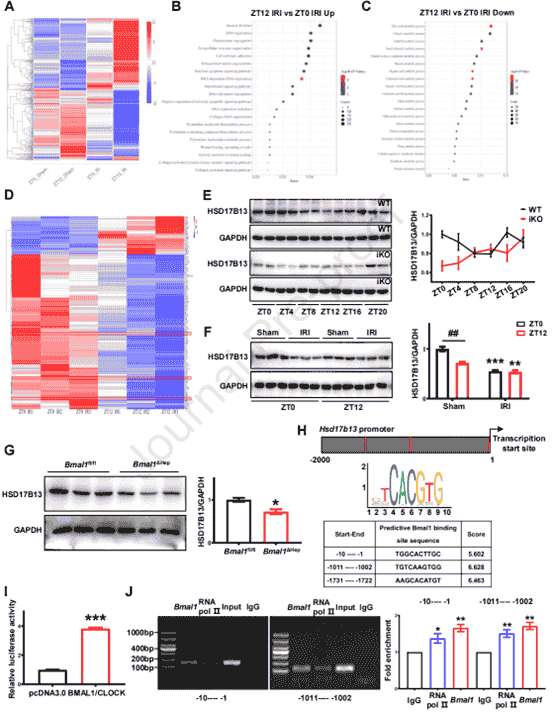
圖4. HSD17B13被確定爲肝細胞中BMAL1的新靶標
4. 肝細胞中Hsd17b13的敲除消除HIRI晝夜差異並加劇肝損傷
基于上述結果,作者利用肝細胞特異性Hsd17b13敲低模型進一步探索了Hsd17b13與HIRI晝夜差異的直接聯系。結果顯示,與肝細胞Bmal1缺失類似,Hsd17b13敲低完全消除了肝損傷的晝夜差異,且ZT0-IRI組小鼠血清ALT/AST顯著升高,肝髒病理損傷加劇,隨之消失的還有肝髒炎症反應和氧化應激的晝夜節律。綜上,肝細胞HSD17B13缺失不僅消除了HIRI損傷的晝夜差異,還特異性地加重ZT0時段的肝損傷,該表型與肝細胞Bmal1敲除高度一致,共同證實BMAL1通過轉錄調控Hsd17b13介導HIRI晝夜節律的假設。
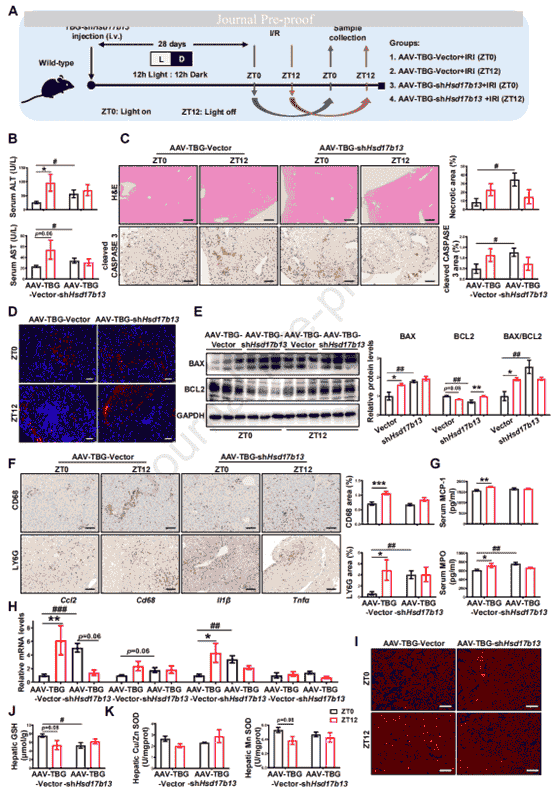
圖5. 肝細胞中Hsd17b13的敲除消除HIRI晝夜差異並加劇肝損傷
5. BMAL1/HSD17B13軸通過促進自噬和減輕脂質積累參與HIRI
爲了更深入地了解BMAL1/HSD17B13軸如何促進HIRI,作者重點研究了HSD17B13在脂質代謝中的作用。結果顯示,HIRI後肝髒脂質顯著積累與損傷程度呈正相關,且具備晝夜依賴性:ZT0時段積累較少、肝損傷較輕,而ZT12時段積累加劇、損傷更重。而肝細胞特異性Bmal1或Hsd17b13敲除均能消除這種晝夜差異,並在ZT0-IRI後加劇脂質積累。體外棕榈酸處理(促進脂質積累)實驗進一步證實BMAL1過表達可緩解脂質過載,而Hsd17b13缺失則加重積累。這些發現強烈提示BMAL1/HSD17B13軸可能在調節肝細胞脂質代謝中發揮保護作用。既往研究表明,自噬在脂質代謝中起着至關重要的作用且遵循晝夜節律。鑒于此,作者檢測了HIRI小鼠肝髒中自噬關鍵標志物的表達,結果表明:HIRI損害自噬通量,表現爲BECLIN1與LAMP1蛋白水平下降、P62與LC3B積累(提示自噬體-溶酶體融合受阻),尤其在ZT12組表現更顯著;Bmal1或Hsd17b13敲除同樣抑制自噬,與脂質積累表型一致。綜上,BMAL1/HSD17B13軸通過調控自噬依賴性脂噬途徑減輕肝髒脂質積累,從而緩解HIRI的晝夜節律性差異。
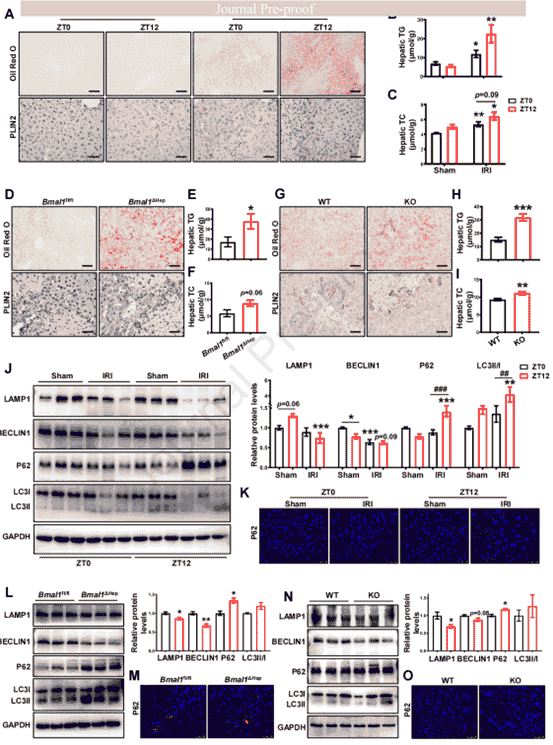
圖6. BMAL1/HSD17B13軸通過促進自噬和減輕脂質積累參與HIRI
6. 肝細胞HSD17B13過表達對HIRI治療的時間依賴性效應
爲探究HSD17B13過表達能否作爲HIRI的治療策略,作者構建了肝細胞特異性過表達hHSD17B13的轉基因小鼠,並實施了IR手術。結果顯示,在ZT0時段,HSD17B13過表達可以顯著減輕肝損傷:血清ALT/AST水平降低,肝壞死面積縮小,凋亡標志物BAX/BCL2比值下降,同時中性粒細胞浸潤減少且炎症因子表達改善。而在ZT12時段,過表達反而加劇損傷,表現爲轉氨酶升高、壞死範圍擴大、促炎因子表達顯著上調。這種晝夜差異提示HSD17B13在HIRI中具有時間依賴的雙重作用,且HSD17B13的肝保護作用嚴格依賴于生物鍾節律。
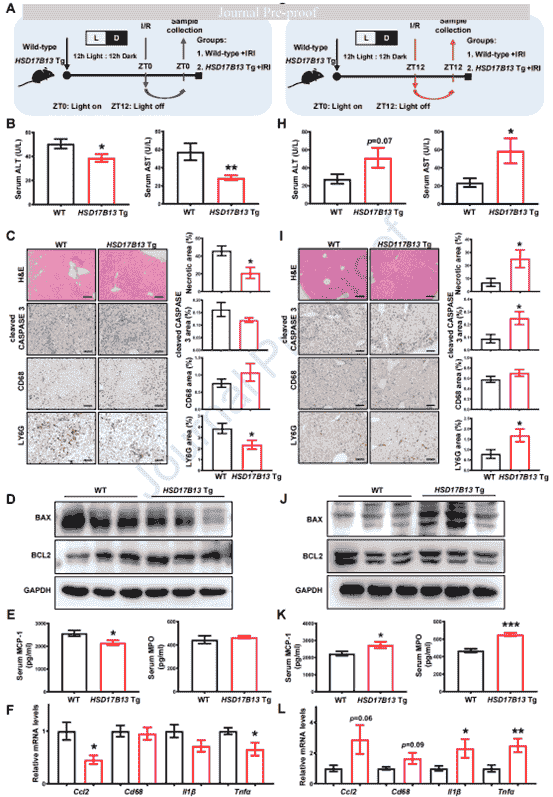
圖7. 肝細胞HSD17B13過表達對HIRI治療的時間依賴性效應
總結
綜上所述,本文首次揭示了BMAL1/HSD17B13軸在HIRI晝夜節律調控中的關鍵作用,通過精確調控BMAL1/HSD17B13軸促進自噬和減少脂質積累可減輕HIRI。這一發現爲臨床肝髒手術和移植提供了重要啓示:通過優化手術時間窗或開發靶向HSD17B13的時序治療策略,可顯著改善HIRI預後。研究首次將生物鍾機制與肝髒缺血損傷的分子病理相聯系,爲時間醫學在器官保護領域的應用提供了理論依據。
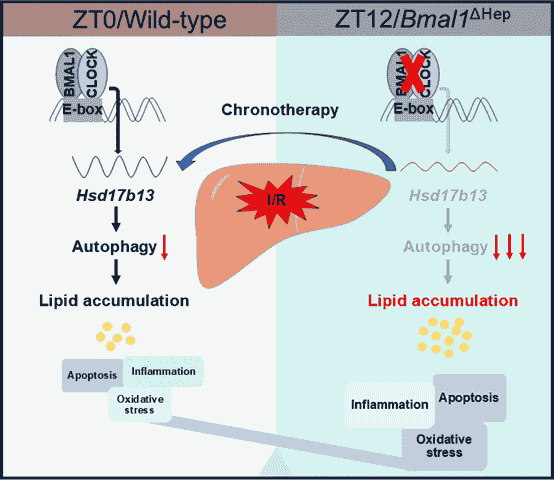
圖形摘要. HSD17B13介導的肝細胞自噬對HIRI的晝夜節律控制

查看更多

查看更多

查看更多

聯系我們公司

返回頂部